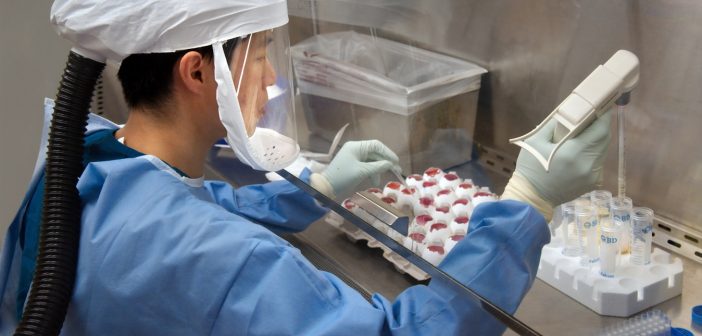
Mahasweta Pal, freelance rédacteur médical at Kolabtree, provides insights into the COVID-19 essai de vaccin à l'Université d'Oxford.
Mise à jour 22/05/2020 : Le vaccin COVID-19 d'Oxford va commencer les essais de phase II/III sur l'homme
Mise à jour 30/12/2020 : Université d'Oxford/AstraZeneca COVID-19 approuvé
Mise à jour 04/08/2021 : Barbie d'Oxford La conceptrice du vaccin Covid Dame Sarah Gilbert a créé
L'année 2020 a marqué le début d'un ralentissement mondial inquiétant, avec le Pandémie de COVID-19, causing mass disruption among soins de santé systems worldwide. Meanwhile, scientists in the United States and Europe jumped into the race to develop and launch vaccines against the pandémie SARS-CoV-2 infection with the shortest timelines. Stalwarts in immunology, virology, vaccinology, épidémiologieet public health ont envisagé les changements massifs requis dans les stratégies de production et de développement des vaccins, en raison de l'émergence des besoins actuels. L'Université d'Oxford a été l'une des premières à susciter l'espoir tout en luttant contre ce défi. Elle a lancé la phase I des essais de son vaccin ChAdOx1 nCoV19 le 21 avril 2020.
Le vaccin ChAdOx1 nCoV19 a été mis au point avec la glycoprotéine (S) du SRAS-CoV-2 ajoutée à la construction ChAdOx1, qui est une version affaiblie d'un virus causant un rhume commun isolé chez les chimpanzés. Les raisons pour lesquelles cet essai est prometteur sont nombreuses, à commencer par le fait qu'il porte sur des volontaires sains (qui n'ont pas été testés positifs à l'infection par le SRAS-CoV-2). Le professeur Sarah Gilbert et son équipe du Jenner Institute ont travaillé sur des maladies virales antérieures, notamment le MERS-CoV et le virus Ebola, et ont mis en œuvre leur technologie d'administration par vecteur adénoviral. Dans une déclaration à The Timeselle a dit qu'elle était 80% confiante dans l'efficacité du vaccin.
Le professeur Sarah Gilbert et son équipe de l'Institut Jenner de l'Université d'Oxford ont commencé à travailler sur les vaccins candidats anti-SARS-CoV-2. aux premiers jours de 2020 alors que seuls quelques cas avaient été signalés à Wuhan. Cette équipe a développé des vaccins contre le MERS et le virus Ebola dans le passé et s'est préparée à répondre à la crise. avant que le nombre total de morts ne dépasse 200 000. Avec l'annonce de la réception des doses de vaccin par les premiers patients de cet essai, une lueur d'espoir semble visible. Voici donc quelques clarifications concernant la conception et d'autres caractéristiques importantes de l'essai.
Quelle est la conception de base du ChAdOx1 nCoV-19 l'essai d'un vaccin candidat ?
L'essai du vaccin ChAdOx1 COVID-19 est un essai en aveugle, randomisé et contrôlé, le vaccin MenACWY servant de contrôle. Les deux premiers patients ont reçu chacun l'un des deux vaccins. L'étude recrute actuellement des participants uniquement dans quatre villes, à savoir Oxford, Southampton, Londres et Bristol. Les deux bras randomisés comprennent 7 groupes qui recevront des doses uniques ou standard de 5×10^10vp de ChAdOx1 nCoV-19 ou du Vaccin MenACWY à la semaine 0qui sera suivie d'une dose de 2,5×10^10vp de ChAdOx1 nCoV-19 à la semaine 4 (dans l'un des groupes expérimentaux).
Pourquoi le vaccin MenACWY est-il utilisé comme témoin ?
Cette étude utilise le vaccin MenACWY comme vaccin "témoin actif", pour aider les chercheurs à comprendre la réponse des participants au vaccin ChAdOx1 nCoV-19. Le vaccin MenACWY est un vaccin homologué contre les bactéries méningococciques des groupes A, C, W et Y. Il est administré systématiquement aux adolescents au Royaume-Uni pour les protéger contre les causes les plus courantes de méningite et de septicémie et est administré comme vaccin de voyage pour les pays à haut risque. La raison de l'utilisation de ce vaccin au lieu d'un contrôle salin est "parce que nous nous attendons à ce que le vaccin ChAdOx1 nCOV-19 entraîne des effets secondaires mineurs tels qu'un bras douloureux, des maux de tête et de la fièvre. La solution saline ne provoque aucun de ces effets secondaires. Si les participants ne recevaient que ce vaccin ou la solution saline de contrôle et développaient des effets secondaires, ils sauraient qu'ils ont reçu le nouveau vaccin." Cela fait partie du processus d'aveuglement visant à garantir que les participants recevant l'un ou l'autre des deux vaccins ne présenteront pas de différences dans leur comportement en matière de santé dans la communauté après la vaccination, ce qui contribue à prévenir tout biais dans les résultats de l'étude.
Le professeur Sarah Gilbert, l'investigateur principal de cet essai d'enregistrement, a également souligné que les critères d'inclusion de l'essai permettront également de comprendre le nombre de porteurs présents dans l'essai puisqu'il s'agit de patients qui n'ont jamais été testés auparavant, ce qui permettra de mieux comprendre les différents niveaux d'immunité après avoir reçu le vaccin.
Quelles sont les mesures des résultats primaires et secondaires de l'essai ?
L'objectif principal de l'étude est d'étudier son action contre le COVID-19, de confirmer qu'il ne provoquera pas d'effets secondaires inacceptables et de vérifier s'il induit des réponses immunitaires raisonnablement remarquables. Essentiellement, les investigateurs principaux vérifieront le nombre de cas symptomatiques virologiquement confirmés (PCR positif) sur une période de 6 mois et l'apparition de symptômes indésirables locaux et systémiques sollicités après la vaccination. Sur la base des résultats obtenus à court terme, les chercheurs procéderont à une analyse plus approfondie des résultats concernant l'efficacité du candidat vaccin ChAdOx1 nCoV-19 contre le COVID-19 sévère et non sévère, sur la base des admissions à l'hôpital, des admissions en soins intensifs et des épisodes d'exacerbation de la maladie..
Dans cet essai, les taux de séroconversion seront également surveillés pendant 6 mois afin d'évaluer si les participants deviennent séropositifs pour les antigènes du SRAS-CoV-2 non-Spike pendant la période d'étude et de quantifier les taux de production d'anticorps chez les participants. La conception de l'essai prévoit également de tester l'immunogénicité cellulaire et humorale du ChAdOx1 nCoV-19 par le biais de tests d'anticorps neutralisant le virus contre le pseudotype vivant et/ou le pseudotype du SRAS-CoV-2.
Quels vaccins ChAdOx ont été utilisés dans les essais cliniques ? Où en sont-ils ?
Les adénovirus, tels que la construction ChAdOx1, sont des vecteurs de vaccins et des véhicules d'administration attrayants car ils peuvent déclencher des réponses immunitaires innées et adaptatives et peuvent être utilisés avec divers antigènes, y compris ceux du paludisme, virus de l'hépatite Ble virus de l'hépatite C et le VIH-1. Le vaccin ChAdOx1 contre le nCoV19 est le troisième vaccin à base de ChAdOx et ses dosages dans les procès en cours ont été décidées sur la base des dosages des précédentes Influenza et Vaccin contre le MERS de 2002 à 2012. Les travaux du professeur Gilbert sur la grippe ont été révolutionnaires car le vaccin développé par son équipe est efficace contre toutes les souches de grippe et induit de puissantes réponses des cellules T pour une protection universelle et à long terme. Le vaccin à vecteur viral a été administré en association avec les vaccins contre la grippe saisonnière pour induire une immunogénicité accrue chez les adultes plus âgés (entre 50 et 85 ans).
Prof. Sarah’s team at the Jenner Institute developed two new simian adenovirus-vectored vaccines (ChAdOx1 and ChAdOx2) and went on to develop viral vectored vaccines against Crimean Congo Hemorrhagic Fever (now in the GMP manufacturing stage), Nipah virus, and Lassa fever, both of which are in the preclinical stage; these vaccine development projects are being pursued in collaboration with Janssen Vaccines & Prevention B.V.& Prevention BV, the vaccine development, production, marketing, and distribution arm of Johnson & Johnson. The ChAdOx1 construct has been used even for vaccines even against Chikungunya and Zika viruses, which are under phase I testing currently. Professor Sarah has led all vaccine projects with respect to the in-house GMP manufacturing, production design, construction, quality control, pre-clinical testing, regulatory and ethical applications to Phase I and II clinical trials at the Jenner Institute.
D'autres exemples de vaccins à vecteur adénoviral ?
Outre les constructions vaccinales à base de vecteur ChAdOx1, le vecteur Modified Vaccinia Ankara (MVA) est un autre vecteur adénoviral non réplicatif qui permet une utilisation plus large parmi de grandes populations avec des profils de sécurité raisonnables et plus durables (6 mois après la vaccination initiale). Pour l'infection par le MERS-CoV, le Jenner Institute vaccins candidats testés basés sur les vecteurs ChAdOx1 et MVA chez l'homme et le chameau dromadaire. Dans la phase I Essai sur le virus Ebola sur 60 volontaires adultes, une dose unique de l'adénovirus 3 du chimpanzé (ChAd3) renforcée par le vecteur MVA a induit des réponses immunitaires 8 fois supérieures. Un site vaccin antigrippal Basé sur le vecteur MNA, MVA-NP+M1 exprime une protéine de fusion de la nucléoprotéine (NP) du virus de la grippe A et de la protéine de matrice 1 (M1). Il présente des effets d'immunisation des cellules T et B contre des antigènes conservés du virus de la grippe et induit des réponses immunitaires humorales accrues.
Comment les effets indésirables seront-ils surveillés cliniquement ?
Les participants recevront un journal électronique "E-diary" pour noter tous les symptômes ressentis pendant 7 jours après avoir reçu le vaccin. Ils ont également reçu l'instruction de noter tous les cas de malaise pendant les trois semaines suivantes. Après la vaccination, les participants se rendront à une série de visites de suivi, qui seront consacrées à l'évaluation des observations cliniques des participants, à la prise de sang et à l'examen du journal électronique. Ces prélèvements sanguins seront utilisés pour évaluer les réponses immunitaires développées au vaccin.
Si les participants développent des symptômes liés au COVID-19 au cours de l'étude, ils sont priés de contacter l'équipe de surveillance de l'essai clinique, qui les examinera pour vérifier s'ils ont été infectés par le virus. Si un participant se sent très mal, l'attention immédiate de l'hôpital sera nécessaire pour examiner le volontaire, le cas échéant.
Financement reçu d'organisations à but lucratif ou non lucratif
Pour ses travaux sur le vaccin anti-SARS-CoV-2, l'Université d'Oxford a conclu un accord avec l'Union européenne. accord avec AstraZeneca AB, qui prendra en charge la fabrication à grande échelle et la distribution éventuelle du vaccin. L'Oxford Vaccine Group de l'université a également reçu 20 millions de livres pour permettre la prise en charge des coûts de production et de distribution pour le Royaume-Uni. The agreement also entails a not-for-profit basis for the duration of the coronavirus pandemic, which covers only the manufacturing and distribution costs. The University and the spin-out company Vaccitech will jointly have the rights to the technology platform used to develop the vaccine candidate and shall receive no royalties from the vaccine during the pandemic. Any royalties received eventually by the University will be reinvested directly into medical recherche, including a newly developed Pandemic Preparedness and Vaccine Research Centre in collaboration with AstraZeneca.
Calendrier possible de la mise à disposition du vaccin
- Sarah Gilbert : ouvrir la voie vers un vaccin contre le COVID-19. Perspectives, The Lancet. 395 (10232) P1247, 18 AVRIL 2020.
- Lancet Infect Dis. 2020 Apr 20. pii : S1473-3099(20)30160-2. doi : 10.1016/S1473-3099(20)30160-2.
- Le vaccin COVID-19 d'Oxford entre dans la phase d'essai sur l'homme. Communiqué de presse de l'Université d'Oxford.
Besoin d'aide pour votre projet sur les coronavirus ? Consultez des virologues, des épidémiologistes et des rédacteurs scientifiques qualifiés sur Kolabtree. Voir nos experts COVID-19